Меланома головного мозга мрт
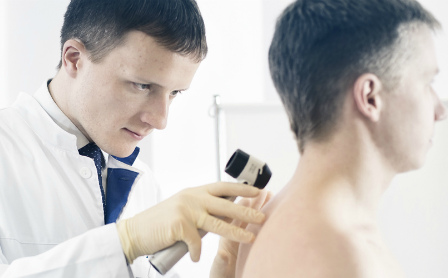
ЛУЧЕВАЯ ДИАГНОСТИКА МЕТАСТАЗОВ В МОЗГ
Метастазы в головной мозг (по данным Б. В. Гайдара, Т. Е. Рамешвили и др.) составляют до 40% всех опухолей, возникающих внутри полости черепа.
ИСТОЧНИК МЕТАСТАЗОВ В ГОЛОВНОЙ МОЗГ
В головной мозг обычно распространяются злокачественные новообразования почек, легких, молочной железы, щитовидной железы, реже — новообразования мочевого пузыря, яичников и простаты. Самая частая ситуация — рак легкого с метастазами в головной мозг. Также склонность к распространению в полость черепа имеют меланомы, практически никогда не метастазируют саркомы. Примерно в 7,8% случаев определить первичную опухоль не представляется возможным.
Частота метастазирования различных опухолей в головной мозг (Б. В. Гайдар, Т. Е. Рамешвили)
| Локализация опухоли | Частота метастазирования |
| Аденокарцинома бронха | 50% |
| Рак молочной железы | 15% |
| Меланома | 10,5% |
| Опухоли органов брюшной полости и таза | 9,5% |
ЛОКАЛИЗАЦИЯ МЕТАСТАЗОВ В ГОЛОВНОЙ МОЗГ
Существуют разные типы расположения вторичных опухолей в полости черепа. Эти типы зависят от того, какие именно структуры поражены. Опухоли метастазируют:
1) В кости черепа
2) В твердую мозговую оболочку. Такой тип распределения вторичных опухолей характерен больше всего для аденокарциномы предстательной железы, светлоклеточного рака почки, меланомы.
3) В мягкую оболочку мозга (синонимы: карциноматозный менингит, карциноматоз мягкой оболочки мозга). Опухоли, чаще всего метастазирующие в мягкую мозговую оболочку: аденокарцинома бронха, молочной железы, желудка
4) Метастазы собственно в головной мозг, в паренхиму головного мозга.
- 80% всех вторичных опухолей локализуются в полушариях мозга
- 15% в мозжечке
- 5% в мозговом стволе
МЕХАНИЗМ РАСПРОСТРАНЕНИЯ ОПУХОЛЕЙ В МОЗГ
Существуют несколько путей распространения раковых клеток по организму. Чаще всего распространение опухоли происходит гематогенным путем (через артериальные кровеносные сосуды). Обычно вторичные опухоли происходят из внутрилегочных узлов (причем, это может быть и первичный рак, и метастаз в легкое). Реже происходит распространение опухолей позвоночника через венозную систему позвонков.
Большое значение в распространении опухолевого поражения имеет спинномозговая жидкость (ликворный путь). Таким образом метастазируют первичные опухоли спинного и головного мозга (медуллобластома, глиболастома, пинеобластома). Возможно также контактное распространение метастатической опухоли по мозговым оболочкам. В некоторых случаях встречается и лимфогенный путь распространения.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ МЕТАСТАЗОВ В ГОЛОВНОЙ МОЗГ
Симптомы при метастазах в головном мозге может быть аналогичны таковым при первичных опухолях, выраженность симптоматики зависит от размера, локализации и количества метастазов, а также от типа их роста, сдавления окружающих мозговых структур, выраженности отека мозговой ткани и т. д.
Наиболее частые симптомы метастазов в головной мозг:
- Парезы и параличи
- Нарушение речи
- Нарушения сознания (помрачнение или отсутствие)
- Судороги (генерализованные или локальные)
- Нарушение психических функций
КТ-ПРИЗНАКИ МЕТАСТАЗОВ В ГОЛОВНОЙ МОЗГ
Как выглядят метастазы в головной мозг на компьютерной томографии (КТ)? Практически во всех случаях выявляется единичное (реже) либо множественные (чаще) объемные образования, которые отвечают следующим параметрам:
- Форма неправильная или сферическая
- Структура неоднородная, в центре очага может обнаруживаться область низкой плотности, обусловленная некрозом и распадом центральной части опухоли. По периферии — более плотный «ободок», который отражает активную часть опухоли, имеющую кровеносные сосуды и обладающую способностью к росту. Этот «ободок» окружен зоной низкой плотности, отражающей отек ткани мозга. Ширина данной зоны может быть различной — от нескольких мм до нескольких десятков см. Относительно однородная структура без наличия участка низкой плотности в центре и без перифокального отека. Такая структура метастаза свидетельствует о его относительной «доброкачественности»
- Отношение к прилежащим мозговым структурам. Очаги могут оказывать объемное воздействие различной степени выраженности на прилежащие отделы мозга, вызывая их смещение. Например, объемное образование в височной доле чаще всего приводит к выбуханию гиппокампа под намет мозжечка (височно-тенториальная дислокация), объемное образование мозжечка может воздействовать на мозговой ствол, приводя к его сдавлению, и т. д. Смерть при метастазах в мозг может наступить в результате сдавления мозгового ствола и нарушения дыхания и сердечной деятельности. В зависимости от локализации, вторичные очаги могут приводить к сдавлению церебральной ликворной системы, приводя к развитию окклюзионной гидроцефалии (резкому расширению центральных ликворных пространств на фоне повышения внутримозгового давления при окклюзии путей оттока ликвора из полости черепа)
- Тип роста. Метастазы могут обладать инфильтративным типом роста (расти, разрушая окружающие ткани) и экспансивным типом (расти, раздвигая окружающие ткани). В первом случае они чаще всего дают осложнения в виде кровоизлияния, то во втором обычно обуславливают возникновение дислокаций.
- Параметры контрастного усиления. Типичные вторичные опухоли в головном мозге увеличивают свою плотность в периферических отделах при внутривенном введении контраста, принимая вид «кольца», «полукольца», «спирали». Гораздо реже наблюдается равномерное контрастное усиление очага. Обычно центральная зона опухоли не усиливается, как и область перифокального отека.
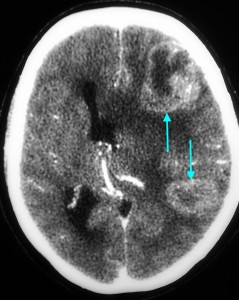
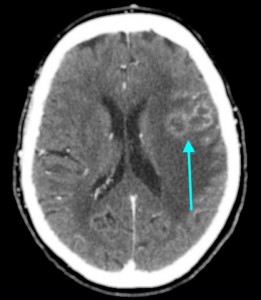
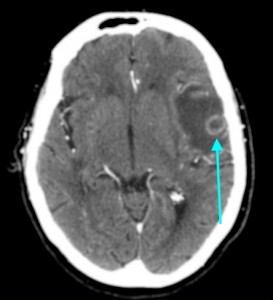
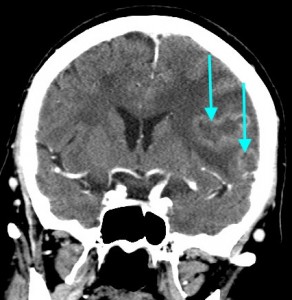
Метастазы головного мозга, фото. На КТ с контрастным усилением у пожилой пациентки (в верхнем ряду слева) с жалобами на головные боли выявлены множественные объемные образования в левом полушарии мозга, интенсивно накапливающие контрастное вещество. Образования имеют характерную форму в виде «кольца». На изображениях в нижнем ряду и вверху справа определяются множественные очаги в головном мозге: отчетливо видны округлые образования с более плотным «ободком» по периферии, располагающиеся в левой теменной доле.
МРТ-признаки метастазов в мозг
МРТ — более чувствительный и специфичный метод в выявлении метастазов ЦНС по сравнению с компьютерной томографией. Вторичные опухоли имеют ряд общих черт при МР-исследовании.
Т1 ВИ (без контрастного усиления)
- Изоинтенсивный либо умеренно гипоинтенсивный сигнал по отношению к белому веществу мозга от активной части опухоли
- Гипоинтенсивный сигнал от центральной зоны (некроза и распада)
Т2 ВИ
- Гиперинтенсивный сигнал от центрального участка метастаза
- Повышение интенсивности сигнала от отечных тканей мозга, окружающих вторичную опухоль, вследствие чего метастазы становятся более четкими на изображениях
МРТ с контрастным усилением
- Выраженное увеличение интенсивности сигнала
- Усиление сигнала по периферии в виде «кольца» или «короны»
- Помогает дифференцировать кровоизлияиния в метастаз от геморрагического инсульта (выраженное усиление сигнала на Т1 ВИ)
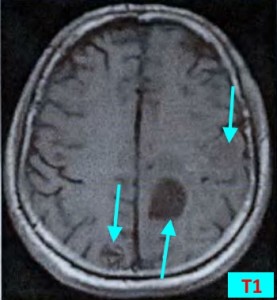
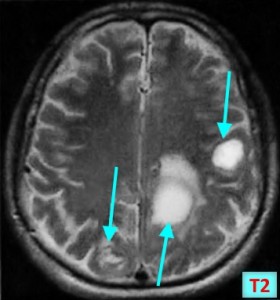
Метастазы головного мозга на МРТ. Фото. Определяются множественные метастазы в мозг при раке легкого: слева в режиме Т1-ВИ в виде гипоинтенсивных образований, справа — в режиме Т2-ВИ виде множественных участков повышенного сигнала, окруженных зоной перифокального отека. У пациента подтверждена первичная опухоль легкого.
Отдельно необходимо рассмотреть МР-признаки метастазов меланомы в головной мозг, которые обладают сигнальными характеристиками, отличающимися от других опухолей вследствие наличия меланина в структуре. Метастазы безамилоидной меланомы выглядят на МРТ аналогично метастазам других опухолей, описанным выше. На Т1-ВИ они имеют резко гиперинтенсивный (высокий, яркий) сигнал, а наТ2-ВИ — изо- либо гипоинтенсивный (пониженный) сигнал.
Позитронно-эмиссионная томография (ПЭТ) в диагностике вторичных опухолей ЦНС
Типичная картина вторичных очагов в головной мозг при ПЭТ — наличие зон повышенного захвата радиофармпрепарата (ФДГ — фтордезоксиглюкоза, либо препаратов меченых аминокислот, таких как метионин) с наличием очагов некроза, протяженных зон отека со сниженным захватом ФДГ.
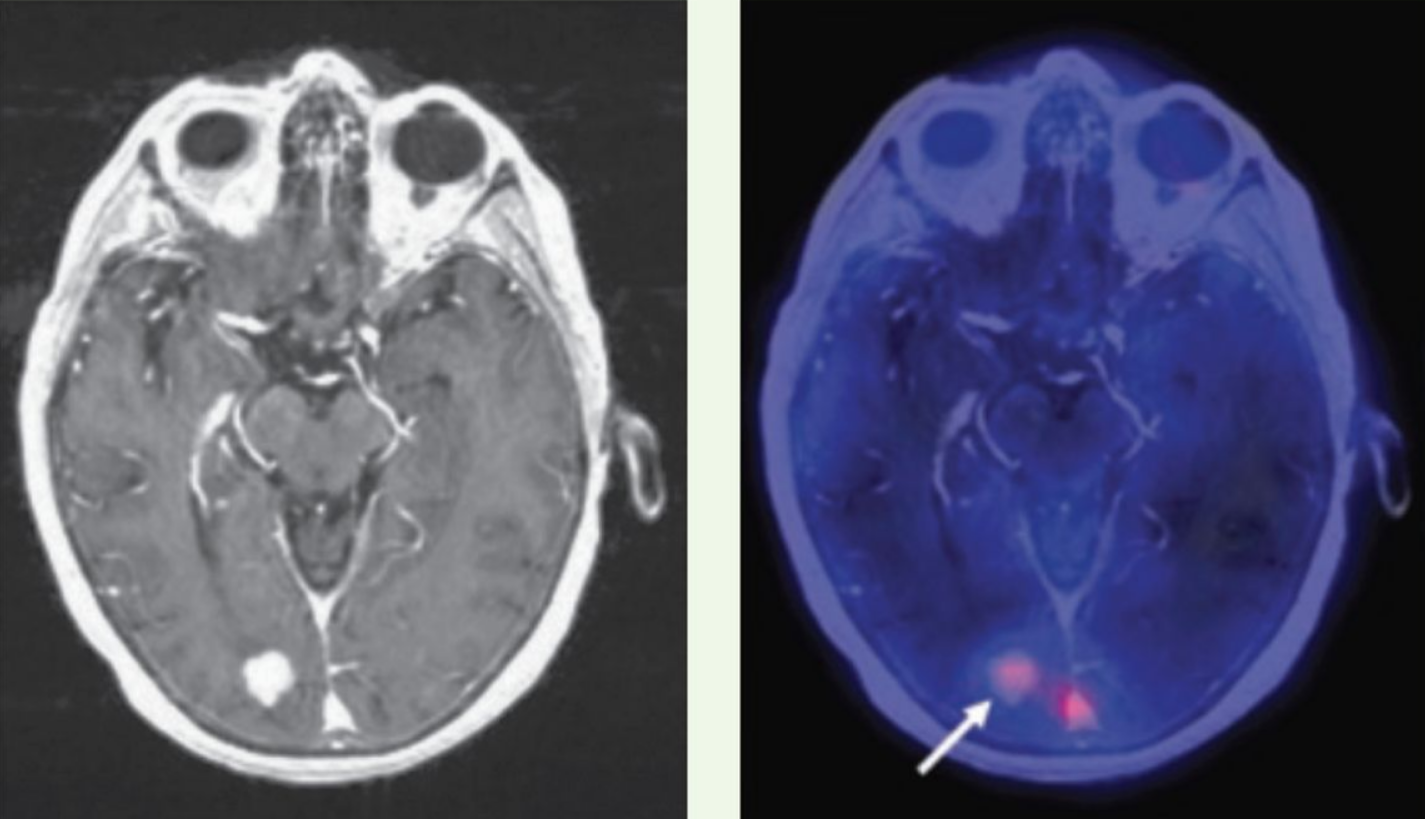
Как выглядят метастазы на ПЭТ-КТ? Здесь виден опухолевый очаг в правой затылочной доле, значительно накапливающий РФП (меченный радиоактивным фтором метионин). ПЭТ-КТ — метод, признанный «золотым стандартом» не только в выявлении метастазов в мозг, но и позволяющий достоверно отличить их от других образований (кисты, абсцессы, гематомы, каверномы и т.п.). От тщательного анализа ПЭТ зависит результат диагностики.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА МЕТАСТАЗОВ В ГОЛОВНОЙ МОЗГ
Одиночные метастазы необходимо отличать от абсцесса, паразитарной кисты, первичной опухоли мозга, лакунарного ишемического инсульта, геморрагического инсульта, рассеянного склероза при обострении процесса. С этой целью необходимо принимать во внимание анамнез заболевания, наличие первичной опухоли другого органа, а также данные методов лучевой диагностики. На первый план выходит не только качество аппаратуры, но профессионализм рентгенолога, оценивающего снимки. Иногда отличить метастазы мозга от других образований бывает сложно, поэтому приходится прибегать к помощи Второго мнения.
ПРОГНОЗ И ПРОДОЛЖИТЕЛЬНОСТЬ ЖИЗНИ У ПАЦИЕНТОВ С МЕТАСТАЗАМИ В ГОЛОВНОЙ МОЗГ
В целом, прогноз при выявлении метастазов в головной мозг является неблагоприятным. Тот факт, сколько живут пациенты с метастазами в головном мозге, во многом зависит от наличия острой симптоматики, обусловленной следующими моментами:
- Сдавление, дислокации и вклинения структур головного мозга
- Вторичный ишемический инсульт либо кровоизлияние
- Перекрытие путей оттока ликвора и развитие внутричерепной гипертензии
- Прорастание в оболочки мозга и кости
- Прорастание опухоли в сосуды мозга
При наличии хотя бы одного из состояний, перечисленных выше, возникает значительный риск для жизни пациента. Наоборот, при отсутствии осложнений, продолжительность жизни даже при наличии метастазов в мозге может быть достаточно длительной и достигать нескольких лет.
МЕТАСТАЗЫ ГОЛОВНОГО МОЗГА — ЛЕЧЕНИЕ
Как лечить метастазы в головной мозг?
1) Хирургическое лечение — удаления образования из ткани мозга может быть показано в случае одиночной опухоли. Решение о том, прибегать или нет к такому лечению, принимает только нейрохирург.
2) Химиотерапия. Адекватно подобранное химиолечение способно значительно увеличить продолжиьтельность жизни даже при отсутствии радикального удаления опухоли. Тип выбранного препарата зависит от гистологического типа первичной опухоли и подбирается химиотерапевтом.
3) Облучение головного мозга при метастазах дает хорошие результаты при наличии хорошей аппаратуры и отсутствии противопоказаний. Вариантами лучевой терапии являются кибернож и гамма-нож. Фактически, здесь речь идет о лучевой хирургии: направленный пучок излучения разрушает патологическую ткань. Показания к этому методу определяются совместно лучевым терапевтом и нейрохирургом.
ВТОРОЕ МНЕНИЕ
Повторная расшифровка результатов КТ или МРТ при метастазах имеет смысл при сомнениях в диагнозе, при необходимости экспертной оценки, при выборе специализированного лечения. Консультирование снимков специализированными рентгенологами в сложных или онкологических случаях стало частью дорогостоящего лечения за рубежом. В России действует Национальная телерадиологическая сеть — служба удаленных консультаций ведущих диагностов, с помощью которой можно получить альтернативное заключение по исследованию (КТ, МРТ или ПЭТ).
Василий Вишняков, врач-радиолог
Читать подробнее о Втором мнении
Читать подробнее о телемедицине

Кандидат медицинских наук, член Европейского общества радиологов
Источник
Пациентка А., 67 лет.
11 июня 2019 пациентка в крайне тяжёлом состояниями была госпитализирована в Европейскую клинику по настоянию родственников. Пациентка была практически недоступна контакту, был отмечен запах ацетона изо рта, в анализе крови от 11.06.2019 обращал на себя внимание уровень креатинина, который составлял 1648 мкмоль/мл.
Родственники предоставили отрывочную документацию, из которой стало ясно, что у пациентки, оперированной в октябре 2014 года по поводу меланомы кожи спины, в мае 2018 года было зафиксировано прогрессирование болезни в виде метастатического поражения левого лёгкого, правого надпочечника, мягких тканей и головного мозга. Учитывая наличие мутации в гене BRAF, с июля 2018 года проводилась таргетная терапия, результатом которой стал полный противоопухолевый эффект в отношении экстракраниальных проявлений болезни и частичный — в отношении метастазов в головном мозге.
Однако уже в марте 2019 года по данным МРТ было отмечено увеличение размеров зоны отёка в веществе головного мозга с возобновлением смещения срединных структур, а также множественный характер поражения данного органа (ранее были описаны только 9 метастазов), на что не обратили внимание ни сама пациентка и её родственники, ни лечащий врач, рекомендовавший продолжить таргетную терапию с контролем через 3 месяца.
Состояние прогрессивно ухудшалось, и в июне уже не могло не тревожить её родных, которые и обратились к нам за помощью. В Европейской клинике пациентке была начата экстренная посиндромная терапия в условиях отделения реанимации и интенсивной терапии, направленная на коррекцию следующих проблем: церебральной недостаточности вследствие метастатического поражения головного мозга, опухолевой интоксикации кахексии, гиповолемии, острого почечного повреждения на фоне хронической почечной дисфункции, выраженной эндогенной интоксикации (гиперазотемии), метаболического ацидоза, разнообразной соматической патологии, в том числе тромбоза вен нижних конечностей. Невзирая на то, что изначально было крайне трудно поверить в конечный успех, уже 18.06.2019 пациентка была переведена в палату с заметным улучшением уровня сознания и активизацией, а также с показателем креатинина 85 мкмоль/мл.
Однако эти клинические успехи явно были только половиной дела. Текущие жалобы уже не были связаны с почечной недостаточностью и интоксикацией, а являлись следствием массивного метастатического поражения головного мозга. По сути, единственным разумным вариантом было начало иммунотерапии, но в таком случае было трудно рассчитывать на мгновенный эффект. По этой причине на фоне первого введения ниволумаба 19.06.2019 уже с 20.06.2019 пациентке был начат курс дистанционной лучевой терапии на весь объём головного мозга. Естественно, мы не могли рассчитывать на значительный противоопухолевый эффект данного варианта лучевой терапии, но надеялись, что его проведение сможет хотя бы немного замедлить прогрессирование опухолевого процесса в головном мозге и даст необходимый запас прочности до начала действия потенциально эффективной иммунотерапии.
Данный комплексный подход увенчался успехом: на фоне начала лучевой терапии состояние пациентки довольно резко улучшилось: она стала активна в пределах палаты, продолжала регрессировать неврологической симптоматики, что, впрочем, могло быть и следствием продолжающейся посиндромной и симптоматической терапии. Данное улучшение состояния довольно скоро сменилось его ухудшением с угнетением сознания и физической активности, а данные МРТ от 05.07.2019 подтвердили наши опасения: было зафиксировано увеличение размеров метастатических очагов и зоны перифокального отёка.
Невзирая на прогностически неблагоприятную ситуацию, общие усилия врачей позволили сдержать планомерное ухудшение состояния на уровне, достаточном для того, чтобы после III введения иммунопрепарата, состоявшегося 19.07.2019, это ухудшение сменилось стабилизацией, а затем и положительной динамикой.
По данным МРТ от 14.08.2019 мы с удовлетворением зафиксировали стабилизацию перифокального отёка и отдельных очагов в сочетании с уменьшением размеров отдельных очагов на 0,2–0,5 см.
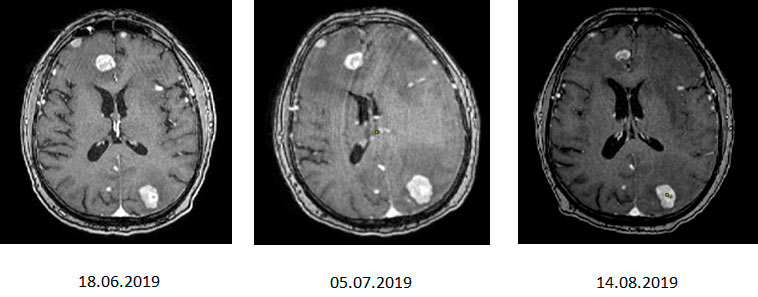
МРТ в режиме Т1 ВИ (после внутривенного введения контрастного препарата), аксиальные срезы. В динамике отмечается сначала увеличение размеров метастазов в веществе головного мозга и перифокального отёка, смещение срединных структур головного мозга вправо; затем уменьшение размеров метастазов и выраженности перифокального отёка, отсутствие смещения срединных структур головного мозга.
Комментирует заместитель генерального директора по научной работе Денис Сергеевич Романов:
После пятого введения иммунопрепарата 14.08.2019 родственники настояли на выписке пациентки, невзирая на предупреждения врачей о том, что ситуация пока далека от разрешения. Уже 18.08.2019 пациентка вновь поступила к нам с жалобами на увеличение в объёме и выраженную отечность правой нижней конечности — и родственники пациентки признали невозможность осуществления необходимого ухода в домашних условиях. После надлежащего вмешательства специалистов состояние пациентки значительно улучшилось, что позволило провести ей очередной курс иммунотерапии ниволумабом, и я надеюсь, что смогу через какое-то время продолжить рассказ о данной клинической ситуации, поведав об очередных успехах этой замечательной женщины в борьбе со столь тяжёлой болезнью.
Источник
Меланома — злокачественная опухоль из меланоцитов, клеток, производящих меланины (белки, защищающие кожу от ультрафиолетового излучения, придающие ей бронзовый цвет при загаре). Локализуется меланома в основном в коже, в более редких случаях может возникнуть в радужной оболочке глаза, слизистых оболочках и очень редко во внутренних органах.
Факторы риска 
Ультрафиолетовое повреждение кожи. Полученные в течение жизни солнечные ожоги значительно повышают риск образования меланомы.
Использование солярия.
Светлый фототип кожи — светлый цвет глаз и волос.
Большое количество родинок.
Более 5 атипичных родинок.
Наличие в личном или семейном анамнезе случаев рака кожи.
Клинически можно выделить 4 основных типа меланом:
Поверхностно-распространенная меланома — один из наиболее распространенных видов меланом, порядка 70% вновь выявленных случаев меланомы. При раннем обнаружении отличается в целом благоприятным прогнозом по сравнению с другими типами.
Узловая меланома – для нее характерен менее благоприятный прогноз, она быстрее растет и чаще метастазирует. В структуре заболеваемости занимает второе место — около 15% всех случаев выявленных меланом.
Акролентигиозная меланома — медленно растущая меланома, поражает чаще всего ладони, подошвы, ногтевые ложа. Порядка 10% среди всех меланом.
Лентигиозная меланома — злокачественный вариант лентиго (описать что такое лентиго), поражает чаще всего пожилых людей, обычно локализуется в области лица, в участках наиболее сильно подверженных инсоляции (воздействию солнца). Растет очень медленно. Прогноз в целом благоприятный, около 5% среди всех случаев меланом.
И наиболее редкая и агрессивная меланома — беспигментная, встречается очень редко, быстро метастазирует, плохо отвечает на терапию, прогноз крайне неблагоприятный, средняя продолжительность жизни у пациентов с беспигментной меланомой — 1-2 месяца.
В целом меланома отличается достаточно агрессивным течением, ранним метастазированием, частым рецидивированием. При этом заподозрить меланому на ранних стадиях во многих случаях достаточно просто, нужно лишь знать, как она проявляется.
Самодиагностика
По всему миру широко применяется ABCDE-система, позволяющая заподозрить наличие меланомы, проанализировав некоторые параметры у подозрительного невуса (родинки). Институт меланомы Австралии, региона, лидирующего в мире по заболеваемости меланомой, разработал специальную учебную программу по профилактике меланомы кожи для учащихся средних школ, программа включает в себя и изучения ABCDE-системы, что подчеркивает важность метода в диагностике и самодиагностике меланомы кожи.
ABCDE – аббревиатура, в которой зашифрованы 5 параметров которые мы должны проанализировать:
A – assymetry, ассиметрия. Мысленно разделите родинку воображаемой линией ровно по середине, если левая и правая половина идентичны — все в норме.
B – borders, границы. У доброкачественного невуса границы края четкие, он четко отграничен от окружающей кожи. У меланомы, напротив, они размыты и могут как бы «врастать» в окружающую кожу.
C – color, цвет. Чаще всего, доброкачественные родинки — одного цвета или оттенка, светлые или темные. В меланоме же могут быть вкрапления синего, красного, желтого и даже зеленого цветов, резко отличающихся от основного цвета родинки.
D – diameter, диаметр. Исследования показывают, что чаще всего, доброкачественный невус характеризуется размерами не более 6 мм, это приблизительно равно размеру круглого ластика на конце простого карандаша.
E – evolution, развитие. Любые изменения происходящие в невусе: изменения размера, цвета, появление сателлитов (небольшие образования схожие по структуре с невусом, появляющиеся вокруг него), появление клинических симптомов — зуд, кровоточивость, покалывание и т.д., все это состояния подозрительные на перерождение доброкачественного невуса в меланому.
Обладая этими знаниями, важно помнить, что окончательный диагноз может поставить только опытный онколог на основании патоморфологического исследования опухоли и полноценного обследования в специализированном центре.
Диагностика меланомы
Ключевым этапом диагностики меланомы является патоморфологическое исследование. Для получения материала опухоль нужно удалить, заранее предполагая, что это может быть меланома, поэтому иссечение должно быть выполнено широко, с захватом окружающих здоровых тканей. В последующем материал отправляется в Гистологическую лабораторию ЕМС, где ведущие российские патоморфологи смогут быстро и точно поставить диагноз. При необходимости, для получения «второго мнения», материал может быть отправлен коллегам из стран Западной Европы и США, эта услуга уже включена в стоимость исследования и дополнительно не оплачивается.
Патоморфологическое и иммуногистохимическое исследования позволяют не только определиться с диагнозом, но и позволят узнать глубину поражения кожи, и наличие у опухоли определенных мутаций, которые окажут ключевое влияние на выбор тактики лечения пациента.
Вторым важным этапом диагностики являются инструментальные и лабораторные исследования, которые нужны для поиска отдаленных метастазов в организме и постановки окончательного диагноза и определения стадии.
Согласно европейским и американским алгоритмам, обследование включает :
КТ органов грудной и брюшной полости, органов таза с внутривенным контрастированием, либо выполнение более совершенного метода обследования — ПЭТ/КТ всего тела, доступного в Институте онкологии ЕМС. ПЭТ/КТ — это современный и точный метод обследования позволяющий за один раз «просканировать» все тело пациента и выявить даже самые небольшие изменения, которые могут быть не видны на КТ.
МРТ головного мозга с контрастированием
При наличии специфических жалоб могут понадобиться дополнительные инструментальные и лабораторные исследования.
Стадирование
 Установка стадии меланомы напрямую зависит от глубины поражения кожи опухолью и наличия метастазов. Цель всех диагностических мероприятий —определить стадию, от этого будет зависеть план дальнейшего лечения.
Установка стадии меланомы напрямую зависит от глубины поражения кожи опухолью и наличия метастазов. Цель всех диагностических мероприятий —определить стадию, от этого будет зависеть план дальнейшего лечения.
Стадия 0 — меланома in situ, опухоль не выходит за пределы эпидермиса.
Стадия I — опухоль толщиной не более 2 мм, нет признаков изъязвления.
Стадия II — опухоль толщиной 1-2 мм с признаками изъязвления, либо опухоль более 2 мм.
Стадия III — опухоль поражает соседние лимфатические сосуды, узлы и/или кожу вокруг себя (появление сателлитов).
Стадия IV — опухоль поражает отдаленные участки организма: печень, легкие, головной мозг и т. д.
Лечение меланомы
Хирургическое лечение меланомы
Выбор тактики лечения меланомы кожи напрямую зависит от стадии заболевания. Когда опухоль локализована только в области первичного поражения (на коже), когда нет сателлитов и отдаленных метастазов (стадии 0, I, II) используются хирургические методы лечения — широкое иссечение + биопсия сторожевого лимфатического узла с последующим патоморфологическим исследованием.
Биопсия сторожевого лимфатического узла — удаление топографически наиболее близкого лимфатического узла к первичному очагу поражения, именно в него сначала устремятся клетки опухоли для метастазирования, и если в узле отсутствуют клетки меланомы — значит опухоль не начала распространение по организму, что дает лучший прогноз для пациента.
У пациентов с меланомой, распространившейся локально, с изменениями в окружающей коже (наличием сателлитов), с пораженными регионарными лимфатическими узлами и сосудами — стадия III — хирургическое лечение дополняется системной терапией (иммунотерапией или химиотерапией). У пациентов с распространенной меланомой — метастазами в отдаленных областях организма — основу лечения составляет системная терапия. Решение о хирургическом вмешательстве принимается в каждом случае индивидуально в зависимости от возможности выполнения операции — состояния пациента и резектабельности метастазов.
Лучевая терапия меланомы
Лучевая терапия — метод лечения меланомы, при котором для уничтожения клеток опухоли применяется излучение с высокой энергией. При лечении меланомы лучевая терапия обычно применяется с паллиативной целью или как метод лечения метастазов в головном мозге, при ограниченных возможностях хирургического лечения, чаще всего для лечения пациентов с меланомой III и IV стадий.
Иммунотерапия меланомы
 Иммунная система — система органов, тканей и специальных клеток организма, основной задачей которых является поиск и уничтожение чужеродных агентов, патогенов, вирусов, паразитов и также опухолевых клеток. Иммунотерапия в онкологии — это вариант системной медикаментозной терапии, направленной на активацию собственной иммунной системы для борьбы с опухолью. Происходит это за счет либо усиления иммунной системы в целом, либо за счет «тренировки» иммунных клеток для лучшего специфического ответа именно против опухолевых клеток.
Иммунная система — система органов, тканей и специальных клеток организма, основной задачей которых является поиск и уничтожение чужеродных агентов, патогенов, вирусов, паразитов и также опухолевых клеток. Иммунотерапия в онкологии — это вариант системной медикаментозной терапии, направленной на активацию собственной иммунной системы для борьбы с опухолью. Происходит это за счет либо усиления иммунной системы в целом, либо за счет «тренировки» иммунных клеток для лучшего специфического ответа именно против опухолевых клеток.
Этот вид терапии на сегодняшний день — один из самых современных и быстроразвивающихся, иммунотерапия становится все более важной частью противоопухолевого лечения. Развитие обусловлено высокой эффективностью таких препаратов, а так же меньшим числом побочных эффектов по сравнению с традиционной химиотерапией. В Институте онкологии ЕМС для иммунотерапии доступны самые новые и качественные препараты, лечение в клинике проводится согласно последним европейским и американским протоколам.
Меланома – иммуногенная опухоль, которая активно борется против иммунной системы организма, ее клетки выделяют специальные вещества, которые позволяют ей либо ускользнуть от иммунных клеток организма, либо за их счет стимулировать собственные рост и развитие.
В иммунотерапии меланомы есть несколько ключевых подходов:
Использование ингибиторов контрольных точек иммунного ответа
Использование цитокинов
Использование таргетной терапии
Использование ингибиторов контрольных точек иммунного ответа
Важной способностью иммунной системы является возможность отличать нормальные здоровые клетки организма от клеток опухоли, происходит это в том числе за счет контрольных точек иммунного ответа – специальных молекул на поверхности Т-лимфоцитов (клеток иммунной системы), которые должны быть активированы или инактивированы для начала иммунного ответа. В терапии меланомы используются блокаторы молекулы PD-1: пембролизумаб (Keytruda) и ниволумаб (Opdivo). Эффективность этих препаратов доказана множеством клинических исследований, при местататической меланоме, более 50% пациентов, получавших эти препараты, переживали 10 лет. Второй группой препаратов в группе ингибиторов иммунных переключателей являются блокаторы CTLA-4 – молекулы, действие которой схоже с PD-1, она также позволяет клеткам опухоли избегать иммунного ответа организма. Основной препарат в группе блокаторов CTLA-4 – ипилимумаб (Yervoy), вещество, также доказавшее свою эффективность в множестве клинических исследований.
Использование цитокинов
Цитокины – химические вещества, которые синтезируются некоторыми клетками иммунной системы. Цитокины играют ключевую роль в регуляции роста и активности иммунных клеток. Для лечения меланомы используют две основные группы цитокинов – интерлейкины и интерфероны.
Интерлейкины – группы цитокинов, которая передает сигналы между иммунными клетками в организме.
Препарат интерлейкин-2 (IL-2) помогает клеткам иммунной системы расти и делиться значительно быстрее. Препарат показал свою эффективность в лечении рака почки и метастатической меланомы. IL-2 может использоваться и в виде монотерапии, и в комбинации с другими препаратами химиотерапевтическими или иммунотерапевтическими. Интерфероны – химические вещества помогающие организму бороться с вирусными инфекциями и опухолевыми клетками. Существует три типа интерферонов: альфа, бета и гамма. Для лечения онкологических заболеваний используется только интерферон-альфа. Он стимулирует активность иммунных клеток и позволяет им эффективнее бороться с клетками опухоли, замедляя их рост и уничтожая их.
Использование таргетной терапии
Терапия моноклональными антителами (таргетная терапия, биотерапия) — вариант системной терапии онкологических заболеваний, при котором используются специально выращенные моноклональные антитела (специальные белки, выделяемые иммунными клетками), тропные именно к клеткам опухоли. Такая терапия подходит не в каждом случае, сначала нужно выяснить гисто-генетический портрет опухоли с помощью иммуногистохимического исследования, которое позволит понять, есть ли в исследуемой опухоли мутации, которые позволят применять таргетные препараты или нет. При выборе тактики лечения меланомы нужно оценить наличие мутаций BRAF, C-kit и MEK, для каждой из них есть свои препараты:
BRAF – вемурафениб (zelboraf), дабрафениб (tafinlar), траметиниб (mekinist) , кобиметиниб (cotellic) — последние два так же активны при наличии мутации MEK
C-kit – иматиниб (gleevec)
К препаратам группы таргетной терапии так же относятся описанные выше блокаторы PD-1. Преимущество моноклональных антител в сравнении с классической химиотерапией в меньшем числе побочных эффектов, достигается это за счет избирательности их действия исключительно на клетки опухоли и в гораздо меньшей степени на остальные клетки организма.
Химиотерапия
Классическая химиотерапия также может применяться при лечении меланом. Обычно это происходит в случаях, когда иммунотерапия оказалась неэффективной, либо если на фоне ее применения развились нежелательные побочные реакции, угрожающие жизни пациента. В лечении меланомы используются химиопрепараты:
Темозоломид
Дакарбазин
Паклитаксел
Наб-паклитаксел
Карбоплатин
Цисплатин
Винбластин
и их комбинации.
Дальнейшее наблюдение
Частота и методы контрольных обследований зависят от стадии заболевания и проведенного лечения. Пациентам с заболеваниями на ранних стадиях (0, I, IIА) показан ежегодный полный осмотр кожных покровов, регулярный самоосмотр кожи и лимфатических узлов. Методы визуализации (КТ, МРТ, ПЭТ/КТ, УЗИ и т. д.) показаны при наличии специфических симптомов.
Пациентам с IIB – IV стадиями заболевания контрольные обследования показаны каждые 3-6 месяцев на протяжении 2 лет после лечения, в последующем — каждые 3-12 месяцев на протяжении 3 лет, и затем каждый год на протяжении всей жизни, регулярные ультразвуковые исследования лимфатических узлов. Обследование включает в себя:
тщательный осмотр кожных покровов и оценку состояния ли?

